|
|

在我们的“外科引流管”系列的第2部分,作者讨论了不同类型引流管的正确放置,放置后如何管理以及何时移除。
在本系列的第1部分,我们讨论了引流管使用的适应症、引流管的类型以及与兽医手术中引流管使用相关的并发症。在第二部分中,我们将讨论不同类型的引流管的正确放置,放置后如何管理,以及何时移除。正确放置对于最大化引流功能非常重要;适当的管理对避免并发症至关重要;并且知道何时移除引流管将确保其不会移除得太早(这会导致液体积聚)或太晚(这会增加感染的风险、增加患者发病率并增加与长期住院相关的成本)。我们将讨论每种引流类型的放置、管理和移除:被动引流、主动引流(Jackson-Pratt,胸廓造口管)和负压伤口治疗(NPWT)。虽然胸腔造口管是一种主动引流管,但技术差异很大,将单独讨论。
被动或主动引流
放置
位置准备
正确放置引流管通常始于手术准备阶段。患者应做好充分的准备(修剪、擦洗和覆盖),以使引流管远离原发切口或伤口。在大多数情况下,在腹膜腔中放置主动吸引引流管不需要额外的考虑,但是许多创伤病例或外科肿瘤病例需要更多的计划,这取决于所使用的引流管的类型。如果使用被动引流,还必须准备好最相关的区域,该区域将用作引流出口。
确定出口位置
在确定引流管的出口点时,需要考虑一些一般规则。 不要通过主切口部位退出引流管。 这样做会为整个切口长度的细菌提供一个进入点,会增加切口感染和裂开的风险,并且如果未来需要进行重建手术,可能会损害组织。更长的皮下隧道可能有助于减少上行感染。
放置引流管
在患者做好准备并确定出口位置后,您就可以放置引流管了。 使用无菌技术,将适当大小的止血钳插入清创的伤口或手术切口。 然后将止血钳的尖端穿过健康的皮下组织并在出口点压在皮肤上。 如果放置腹腔引流管,止血钳会被直接强制穿过体壁(图 1A)。 使用手术刀刀片,在止血钳的尖端做一个小切口,然后将止血钳推入刺入切口(图 1B)。 切口的大小应与主动引流管的直径相同或略大于被动引流管的直径。 然后抓住引流管的末端并将其拉入伤口或腹腔(图 1C)。 当您将引流管从出口部位拉出时,用无菌盐水预先润湿引流管有助于减少摩擦。
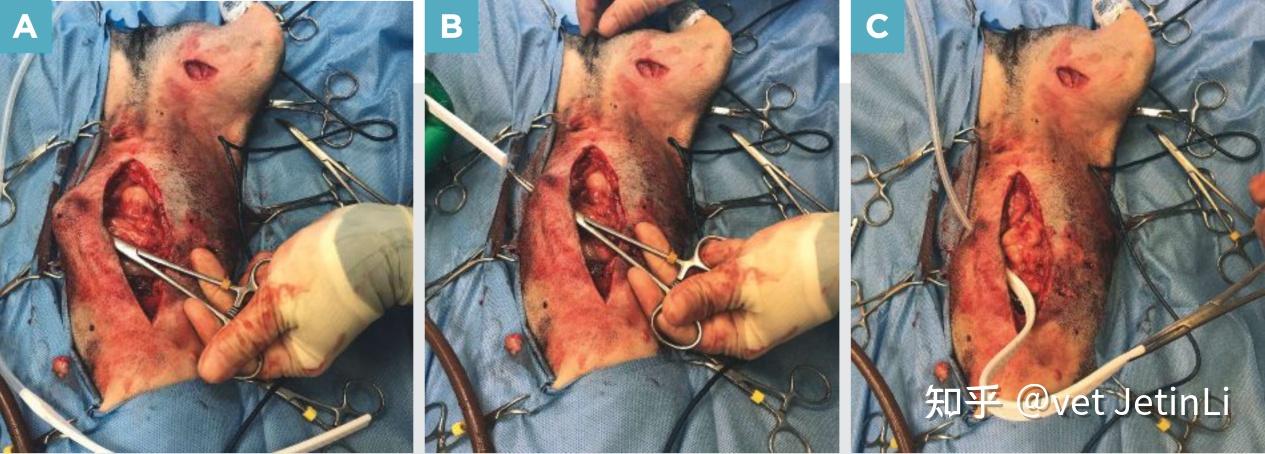
图 1. 在腹腔内放置一个封闭的吸引引流管。 (A) 将止血钳放置在腹膜腔中。 引流管被直接推过体壁并推到皮肤上。 (B) 在止血钳上做一个刺切口,并将止血钳推入刺切口。 (C) 抓住引流管并将其拉过皮肤、皮下组织和肌肉; 然后将其放置在腹膜腔内。
固定引流管
为了使引流管正常工作,固定它是至关重要的。被动引流在出口处用1或2个简单的间断缝合线固定。主动引流管通常用荷包缝合以形成密封,并用指套缝合将其固定在适当的位置(图2、3)。
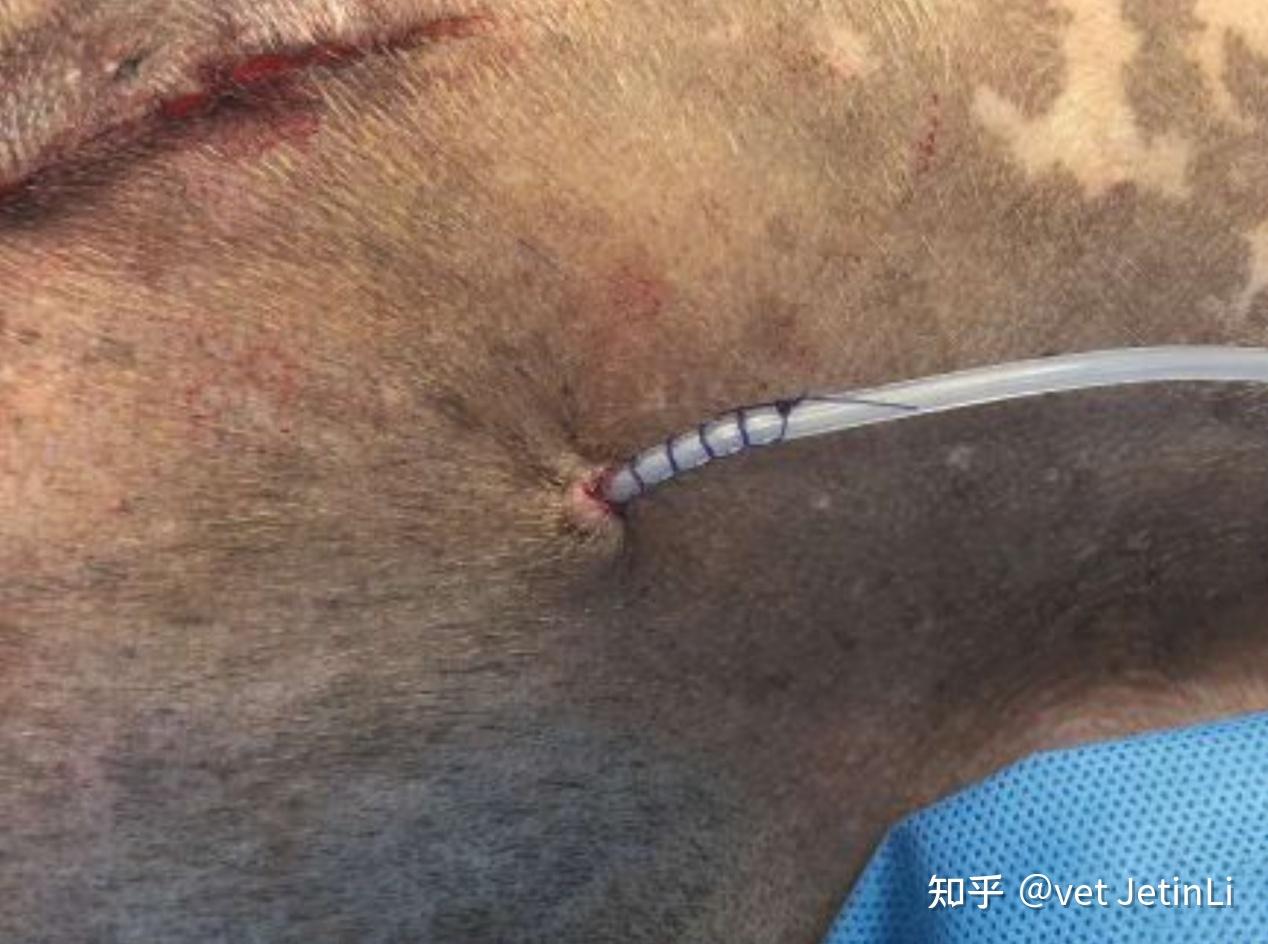
图 2. 封闭式吸引引流管的出口正确放置在远离主要切口的位置。 注意引流口附近荷包缝合处的皮肤压痕。 还可以看到将引流管固定到位的指套缝合。
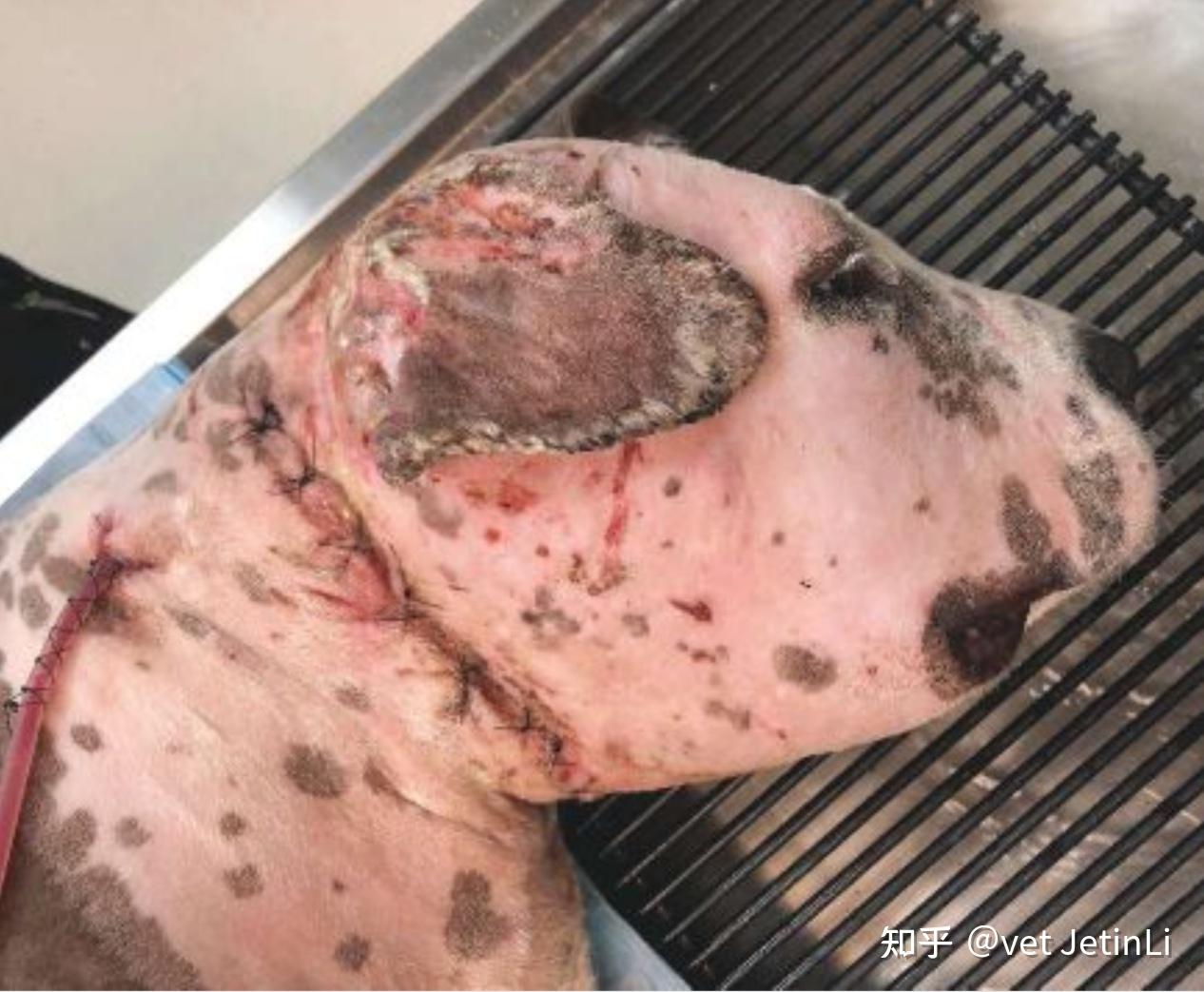
图3.一个封闭的吸引流管到位。注意引流管远离主要伤口闭合处的位置以及指套缝合。
关于在伤口内固定被动引流管的近端部分存在一些争议。不推荐额外的定位缝合,并且通常是禁忌的,因为它们产生引流管破裂或撕裂的风险,在伤口中留下碎片。如果绝对必要,你可以在引流管的近端放置一个简单的经皮间断缝合来固定它。这种缝合线应该在病历中清楚地指出,以便所有人员都知道它的存在,并且可以避免在未切断所有缝合线将其固定到位的情况下拉动引流管的任何部分在伤口内断裂。
保护引流管
无论引流管类型如何,出口部位都应覆盖无菌吸收敷料,以最大限度地降低上行感染的风险,收集渗出物,并防止表皮脱落。这种覆盖对于被动引流尤为重要。在不适合包扎的身体部位,可以在出口处放置一个捆绑绷带,并根据需要经常更换,以防止穿透。
管理
细菌定植的风险随着引流管放置时间的延长而增加; 因此,应尽早拆除引流管。要确定何时可以拆除引流管,请每天一次或多次评估液体的质量和数量。 更换绷带、清洁引流出口和清空引流容器时,请遵循无菌技术。
在封闭的抽吸引流管中,例如Jackson-Pratt引流管,抽吸用于从伤口或腹部抽出液体。抽吸可以是连续的或间歇的;然而,持续抽吸是最常用的,也是推荐的。持续抽吸可最大限度地减少静态液体中机会性细菌引起的感染。对于间歇性抽吸,建议每 6 小时对储液罐进行一次无菌清空;然而,对于非常严重的伤口,可能需要每小时更换一次储液器。
主动引流依靠在引流出口处有一个密封件来保持负压。如果引流出口太大,如果荷包缝合不到位,或者如果主切口裂开,空气会被吸入伤口,负压会丧失。对于通过切口或引流出口的轻微泄漏,可以使用抗生素软膏和封闭敷料来密封泄漏。对于较大的泄漏,可能需要压缩绷带来形成密封。在一些切口裂开的病例中,需要进行手术修正。
大多数市售的主动引流系统都有可压缩的储液罐。为了产生负压,排空容器,然后用手压缩容器,通过打开的通风口排出空气。排气孔然后被封闭,因此负压被施加到引流管,并且储存器自然膨胀。一项体外研究表明,当可压缩容器填充至20%至30%容量时,其吸力会迅速丧失,随着进一步填充,吸力会逐渐丧失,并且一些装置在充满之前会丧失所有吸力。因此,如果预计会有大量液体,建议使用更大的容器,并且容器半满时应清空。
移除
引流管移除的时间取决于液体的数量及其细胞学外观。
产生的液体量不仅可以指示何时可以移除引流管,还可以指示问题。为了评估被动引流管的液体量,在放置绷带之前和之后称量绷带材料将使您大致了解吸收了多少液体。不幸的是,通过绷带的蒸发使称量绷带成为液体生产的粗略指标。使用主动抽吸引流管可以更精确地评估液体量。每次清空储液器时,应量化并记录液体量。请注意,当引流管就位时,液体的产生永远不会停止,因为引流管的存在会导致组织产生液体。作为一般规则,引流管的存在将导致产生 1 mL/kg/天的液体,这个数字通常用于确定何时应移除引流管。 然而,更常见的是,当液体产量显着减少时移除引流管,并且几天的趋势表明液体产量正在减少,而不是等到体积已达到 1mL/kg/天的阈值。
液体质量
从引流管收集的液体的细胞学外观可用于评估伤口愈合的进展。 从被动引流管收集液体时,将无菌采血管放在引流管下方以收集一些积液。 对于主动引流管,将新的无菌注射器直接连接到引流管,而不是收集已在引流管中长时间放置的液体。 在愈合组织中,整体细胞结构应减少,中性粒细胞的外观应从毒性或退化改善为保存完好且不退化。
还可以评估细菌的存在;然而,细胞学样本中没有细菌对于排除感染并不是100%敏感的。对于腹腔引流液,如果担心腹膜腔内的持续感染或新感染,您可以将引流液中的葡萄糖和乳酸盐水平与外周血中的进行比较。与外周血糖相比,腹部葡萄糖下降超过20 mg/dL对于诊断狗的脓毒性腹膜炎具有100%的敏感性和100%的特异性,对于诊断猫的脓毒性腹膜炎具有86%的敏感性和100%的特异性。在狗中,血液和体液乳酸水平差异小于或等于 2.0 mmol/L 对诊断脓毒性腹膜炎也具有 100% 的敏感性和特异性。
程序
无论是被动引流还是主动引流,拆除时都要切断用于固定引流的缝线,并轻轻牵引以将其拆除。尽管拔除引流管对病人来说是不舒服的,但很少需要镇静。让引流出口伤口保持开放以二期愈合。为防止上行感染,在接下来的3至5天内应用软垫绷带;你也可以涂一层薄薄的抗菌软膏。如果引流管被放置在感染的伤口中,在移除引流管时进行第二次培养以确保现有感染得到解决。
胸廓造口管
放置
当需要以频繁间歇或连续的方式清除大量空气或液体时,胸腔造口管是必要的。它们也可用于胸部手术后的局部麻醉。胸廓造口导管应该是柔性的,但要抗塌陷。放置导管时,采用无菌技术,患者通常侧卧。在大多数情况下,这些管子是在病人全身麻醉下放置的;然而,在紧急情况下,可以通过镇静或局部麻醉来完成的。对该区域进行备皮、擦洗和消毒。理想地,管应该在第二肋附近终止;你应该预先测量导管,以防止它进入头侧纵隔。在将胸腔造口术导管插入胸腔之前,放置一个专门用于胸腔导管的管夹。在第10或第11肋间水平的胸腔背侧三分之一处开一个小切口,大约为导管的直径。然后在皮下组织中制造一个隧道,以提供限制空气进入胸膜空间的“瓣阀”效应。隧道也深至背阔肌的尾侧边缘。这条隧道可以用多种方式建造。在进行最初的皮肤切口后,将皮肤向颅侧回缩至第七或第八肋间隙的水平,使用大型止血钳从皮肤切口处形成隧道,然后将导管在第七或第八肋间隙的水平处插入胸腔。最后,胸廓造口术导管和套管针可用于建立隧道并进入胸腔。使用胸廓造口术导管和套管针进入胸膜腔需要很大的力量。我们建议将一只手放在导管远端,距离患者身体约2-3cm;这只手将防止导管进入胸腔太深而对胸腔内器官造成损伤。一只手放在导管的远端,另一只手用力进入胸腔。导管进入胸腔后,将套管针对准对侧肘部并保持在固定位置,同时推进胸腔造口术导管。
拔下套管针时,使用预先放置的夹子或止血钳压缩胸廓造口术导管,并用适配器和旋塞阀装置盖住导管末端。为了避免穿孔移位或胸膜外移位,通过在出口部位的皮肤上放置荷包缝合线以形成密封,并以指套缝合的方式进行第二次缝合,从而将胸廓造口管固定到位。然后用注射器手动排空胸膜腔,直到达到负压。拍摄术后x光片,以确保引流管放置恰当。使用无菌纱布和小绷带覆盖可用于防止医院内感染,或者如果需要覆盖额外的伤口,可使用较大的绷带。矫形金属丝通常用于连接适配器和旋塞,以确保它们不会被意外移除,否则会导致突发性气胸。
管理
对于无生命危险的空气或液体积聚,间歇抽吸就足够了;然而,对于气胸、乳糜胸或脓胸的内科治疗,持续引流可能是必要的。为了预防危及生命的医源性气胸,所有参与胸腔造口管引流的人员必须经过适当的培训。在两次抽吸之间,用金属C形夹(或预置的塑料夹)压缩夹子,用适配器密封,并用三通旋塞盖住,以降低抽吸之间空气进入的风险。分别记录每个胸腔造口管的空气和液体量。抽吸的频率通常在最初几个小时每小时都很高,然后随着液体和空气积聚的减少以及患者临床症状的缓解而逐渐降低。
移除
当漏气处出现密封、液体量明显减少和/或液体的细胞学外观似乎有所改善且无感染迹象时,可移除胸廓造口导管。移除胸廓造口导管的标准与闭合吸引引流管的标准相似。
负压伤口治疗
NPWT指的是泡沫敷料的应用和均匀分布在伤口上的负压的使用。使用NPWT的理想伤口是那些由外伤引起的高渗出性伤口。无论在伤口上使用何种敷料,负压治疗的伤口准备原则都是相同的:清除坏死组织和失活组织并进行大量灌洗。
放置
如果应用不当,管理NPWT可能会令人沮丧;因此,最初小心谨慎地使用敷料可以节省大量的时间。典型地,当患者处于全身麻醉时应用NPWT;然而,随后的再次应用只能在患者处于镇静状态下进行。NPWT的应用和更换应采用无菌技术。在使用泡沫敷料之前,在伤口周围至少3~5cm的范围内,用宽的边缘夹住并擦洗伤口,以便与粘性布充分接触。对于伤口周围皮肤的最后擦洗,使用酒精,这将有助于作为干燥剂。为了使粘性盖布与皮肤接触并形成密封,在应用NPWT之前,伤口周围的皮肤完全干燥是非常重要的。
在伤口准备、清创和干燥后,在伤口周围3~5cm的皮肤上涂一层薄薄的液体皮肤粘合剂。如果伤口负压应用于不平坦的表面(例如,手指之间),人造口糊剂或水胶体凝胶可以模制成坝,以帮助确保气密密封。切割泡沫敷料以适合伤口(图4A),注意不要将泡沫应用于皮肤。如果将NPWT应用于移植物,切割泡沫以覆盖切口。为了保持泡沫在适当的位置,你可以使用缝线或皮肤钉将泡沫固定在自身或患者的皮肤上。将泡沫敷料贴在伤口上后,用不透水的粘性布封住整个区域(图4B)。小心避免褶皱或折叠,因为它们会阻碍气密密封的形成,并损害敷料的完整性。
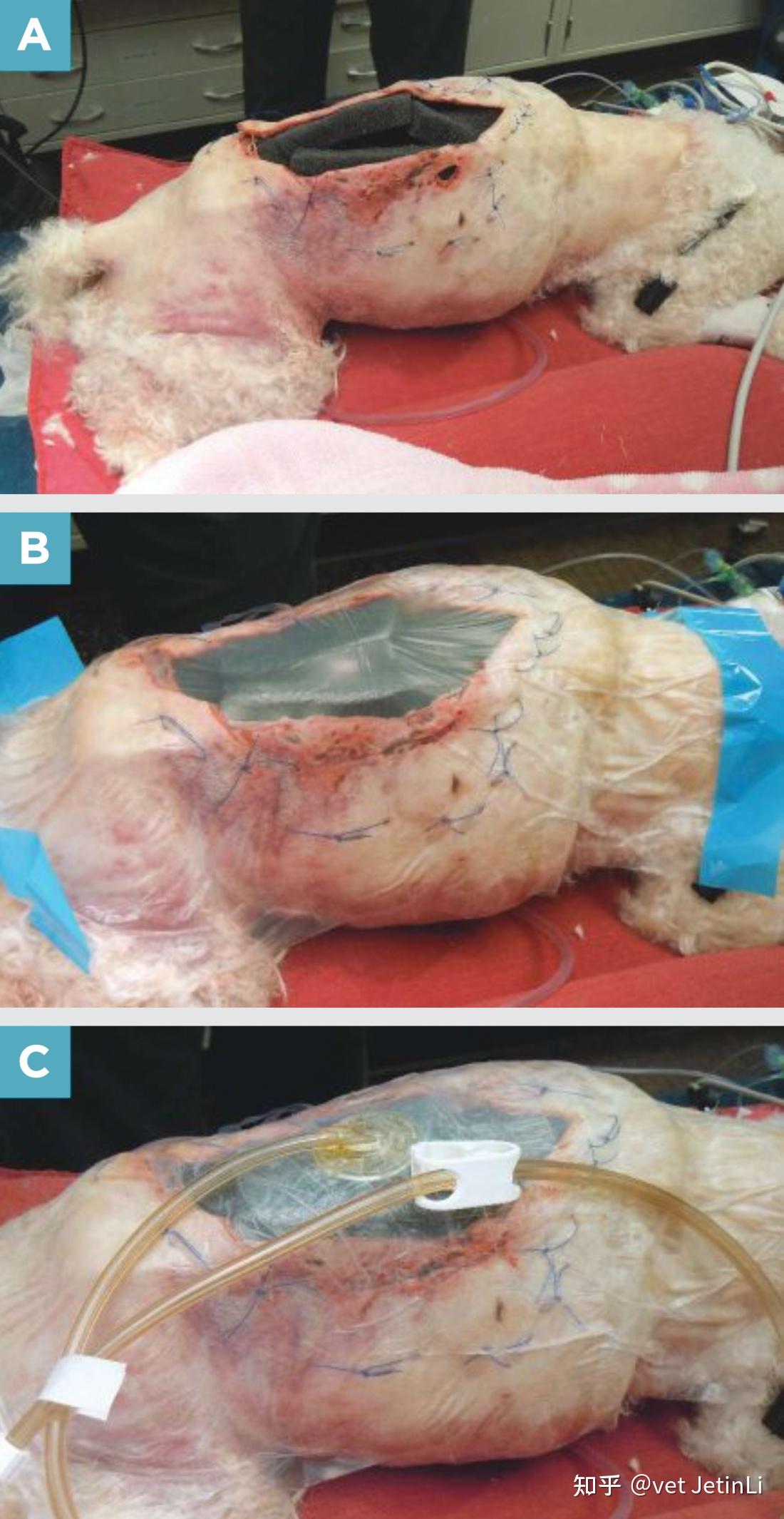
图4.在大伤口中放置开孔泡沫。(A)泡沫在伤口内,避免与皮肤的任何接触。(B)放置粘性不渗透的布帘。(C)连接管道的演示。与图B的比较表明,泡沫是塌陷的,并且建立了负压。
为了放置与抽吸管相关的专有带孔粘合盘,在覆盖伤口的片材上切一个2cm的小圆孔,露出泡沫敷料区域。然后将抽空管(图4C)连接到可编程负压泵的储罐上。泵通常可以设置为-75~-125mmHg范围内的间歇或连续负压。狗可以忍受间歇或连续治疗;然而,猫有时似乎不喜欢间歇模式下负压的重新启动。对于移植物上应用的NPWT,我们建议将压力设置为-75mmHg。当泵达到其预设的负压水平时,它变得安静并且仅间歇地激活;仔细听泄漏的声音,并根据需要添加更多的粘性覆盖物。如果将伤口负压放置在肢体上,可以将管道盘绕起来,并使用软垫绷带。大型犬可以穿背心,负压泵可以随身携带。对于小型犬猫,负压泵放在笼子外面;遛狗的时候可以带着泵。
管理
对NPWT来说,伤口需要每48~72小时重新包扎一次。敷料放置的时间不应超过72小时,因为肉芽组织可能会生长到泡沫的空隙中。更换敷料时保持无菌技术是很重要的。可以移除整个粘性盖布和泡沫,或者仅移除泡沫上的部分。冲洗伤口后,在原来的消毒盖布上放上新的泡沫和粘性消毒盖布。
应密切监控敷料完整性和机器功能;这种泵被设计成在失去压力时触发警报。如果失去负压超过2小时,敷料将变得闭塞,并将发生伤口浸渍。
移除
当NPWT用于急性创伤伤口时,在健康的肉芽组织出现之前,通常只需更换1~3次绷带。在存在健康的肉芽床之后,可以移除伤口负压,并且可以继续伤口包扎,以允许伤口边缘的二次愈合和闭合,或者可以应用皮肤移植来闭合缺损。
要点
- 尽管引流管的使用是伤口护理的一个非常有用的部分,但它们的使用不能弥补不充分的清创术、不适当的伤口护理或不适当的外科技术。
- 对于被动引流,出口部位应该是患者最受影响的区域。
- 被动引流管应覆盖适当的绷带,以尽量减少并发症。
- 对于主动引流管,适当的固定和密封对功能至关重要。
- 应密切监测NPWT,以避免负压损失超过2小时,从而导致伤口浸渍。
- 引流移除的时间应基于液体的数量和质量。
参考文献
- Campbell BG. Bandages and drains. In: Tobias K, Johnston S, eds. Veterinary Surgery: Small Animal. 1st ed. St Louis, MO: Elsevier; 2012:221-230.
- Bonczynski JJ, Ludwig LL, Barton LJ, et al. Comparison of peritoneal fluid and peripheral blood pH, bicarbonate, glucose, and lactate concentration as a diagnostic tool for septic peritonitis in dogs and cats. Vet Surg 2003;32(2):161-166.
- HungGC,GauntMC,RubinJE,etal.Quantificationand characterization of pleural fluid in healthy dogs with thoracostomy tubes. Am J Vet Res 2016;77(12):1387-1391.
- Stanley BJ. Negative pressure wound therapy. Vet Clin North Am Small Anim Pract 2017;47(6):1203-1220.
附加资源
Radlinsky MG. Thoracic cavity. In: Tobias K, Johnston S, eds. Veterinary Surgery: Small Animal. 1st ed. St. Louis, MO: Elsevier; 2012:1796-1798. |
|