|
|
今天给大家介绍的是NATURE REVIEWS DRUG DISCOVERY杂志于2018年发表的综述《Drug repurposing: progress, challenges and recommendations》。第一作者为Sudeep Pushpakom,来自于利物浦大学。
导语
尽管现代科学进步飞速,但是这些给药物开发带来的好处远远低于预期。全球制药行业面临的挑战是多方面的,包括高流失率,超长的临床试验周期,以及不断变化的监管要求,这些都可能导致更高的成本。药物再利用(也叫药物再定位,重新定位或重新分配任务)是一种为已批准或正在研究的药物确定新用途的战略。
与为特定适应症开发一种全新的药物相比,这种策略具有许多优势。首先,失败的风险较低;因为重新利用的药物已经被发现在临床前模型和临床应用中具有足够的安全性。如果早期阶段的试验已经完成,在临床前模型和人体中已经确定有足够的安全性,因此至少从安全的角度来看,它在随后的试验中失败的可能性较小。第二,药物开发的时间可以缩短,因为大部分的临床前测试、安全评估以及在某些情况下的制剂开发都已经完成。第三,投资减少,尽管这将根据再利用候选药物的开发阶段和过程而有很大不同。对于再利用的药物,其监管和第三阶段的成本可能与相同适应症的新药大致相同,但仍可在临床前和临床一期和临床二期上节省大量资金。药品开发的风险更小,投资回报更快,而且一旦失败,平均相关成本也更低。历史上,药物的再利用在很大程度上是偶然的;一旦发现一种药物具有脱靶效应或新发现的靶效应,它就被推进商业开发。比如,西地那非(伟哥)最初是作为一种抗高血压药物开发的,但是偶然发现其有治疗勃起功能障碍的作用。但当被辉瑞公司重新用于治疗勃起功能障碍并作为伟哥上市时,它在勃起功能障碍中占市场领先了47%。
这些成功也鼓励了开发更系统的方法来确定可再利用的化合物。在这篇综述中,作者概述了各种帮助药物重新利用的方法,包括对新类型的大数据的使用,还讨论了所遇到的主要挑战,以及提出了可以加速实现药物再利用潜力的建议。
药物再利用的方法
2.1 计算方法
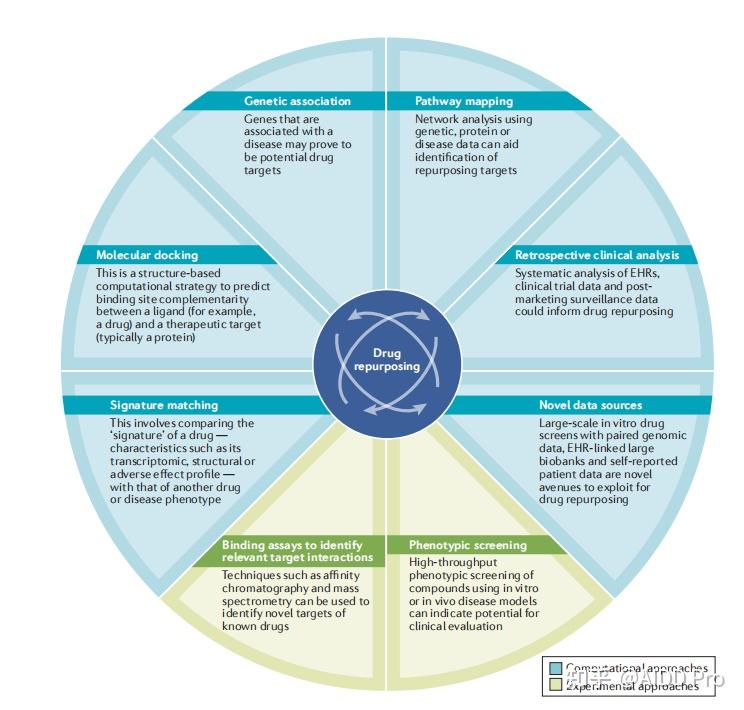
计算方法主要以数据为驱动;它们涉及许多类型数据的系统分析(如基因表达、化学结构、基因型或前基因组数据或电子健康记录(EHRs)),然后可能导致重新利用的假设(图1)。下面将讨论最常用的计算方法。
2.1.1 特征匹配
特征匹配是基于对一种药物与另一种药物、疾病或临床表型的独特特征或“特征”的比较。药物的特征可以从三种一般类型的数据中获得:转录组学(RNA)、蛋白质组学或代谢组学数据;化学结构;或不良事件概况。匹配的转录组特征可用于进行药物-疾病比较(估计药物-疾病相似性)和药物-药物比较(药物-药物相似性)。在第一种情况下,特定药物的转录组特征是通过比较药物治疗前后的生物材料的基因表达谱,如细胞或组织的基因表达谱;然后,将所产生的差异基因表达特征(药物的分子特征)与通过疾病与健康条件的差异表达分析同样获得的疾病相关表达谱进行比较。这种计算方法依赖于特征逆转原则(SRP),即假定如果一种药物能够逆转作为特定疾病表型标志的一组基因的表达模式(也就是说,药物特征将更接近于健康状态下的表达模式),那么这种药物可能能够逆转疾病表型本身。尽管这一原则相当简单,但它已被证明适用于代谢性疾病,并被成功地用于在广泛的治疗领域确定新的药物重新定位的机会。第二种情况,药物间的相似性方法旨在识别本来不相似的药物(属于不同类别或结构不相似的药物)的共同作用机制,可以帮助识别现有药物的替代靶点,并发现潜在的非靶点效应,从而为临床应用进行研究。因此,两种药物之间共同的转录组特征可能意味着它们也有共同的治疗应用,而不管其化学结构的相似性或不相似性(见BOX 3中法舒地尔的案例研究)。这一原则已被证明是有效的。
2.1.2 计算分子对接
分子对接是一种基于结构的计算策略,用于预测配体(例如药物)和靶点(例如受体)之间的结合点互补性。如果事先知道一个疾病涉及的受体靶点,那么可以针对该特定靶点对多种药物进行测试(常规对接:一个靶点和多个配体)。反之,可以针对一系列目标受体探索药物库(反向对接:几个目标和一个配体),以确定可用于重新使用的新的相互作用。利用高通量计算对接,Dakshanamurthy及其同事对2,335个人类蛋白质晶体结构中的3,671个FDA批准的药物进行了分子配合计算。他们发现麦苯达唑,一种抗寄生虫的 药物,具有抑制血管内皮生长因子受体2(VEGFR2)的结构潜力。
2.1.3 全基因组关联研究
全基因组关联研究的数量已经有了很大的 随着基因分型技术的进步、人类基因组计划的完成和基因分型成本的降低,过去10年进行的全基因组关联研究(GWAS)的数量大幅增加。GWAS旨在确定与常见疾病相关的遗传变异,从而提供对疾病生物学的见解;获得的数据也可能有助于确定新的靶点,其中一些靶点可能在药物治疗的疾病和GWAS研究的疾病表型之间共享,从而导致药物的重新定位。
2.1.4 路径或网络图谱
基于路径或网络的方法已被广泛用于识别可能具有再利用潜力的药物或药物目标。如上所述,即使通过GWAS或其他方式发现的一些潜在靶点可能使自己直接成为药物靶点,但很多时候,这些基因可能不是理想的可药用靶点。在这种情况下,基于路径的策略可以提供有关基因的信息,这些基因是GWAS的上游或下游。处于GWAS相关靶点的上游或下游的基因的信息,并且可以利用这些基因进行药物再利用。
2.1.5 回溯性临床分析
使用电子健康记录。西地那非是回顾性临床分析导致候选分子重新使用(或在药物主要适应症失败的情况下进行挽救)的最好例子。其他通过回顾性临床和/或药理学分析产生的再利用机会的例子包括阿司匹林在结直肠癌中的应用(美国预防服务工作组于2015年9月发布了关于使用阿司匹林帮助预防心血管疾病和结直肠癌的建议草案),拉罗昔芬在乳腺癌中的应用(Evista; 美国食品和药物管理局批准用于降低未被诊断但患病风险高于平均水平的绝经后妇女患激素受体阳性乳腺癌的风险)。然而,以上所举的例子并不是因为对临床数据的系统分析而产生的。现在越来越多的人建议采用系统的方法来分析临床数据,以确定药物再利用的机会。
2.1.6 用于药物再利用的新的数据来源
永生化的人癌细胞系(CCLs)已被用于针对数百种化合物(包括已批准的和试验性的)的高通量药物筛选,以测试它们对细胞活力的影响。在一些研究中,这些筛选产生的药理学数据集已经与被检测的CCLs的综合基因组特征配对,从而允许识别细胞的分子特征和药物反应之间的相互作用(药物基因组学相互作用)。挖掘这类公开的数据集,其中包含大量的基因组和药理学数据。CCLs被认为是识别药物重新定位机会的一种新资源。
2.2 实验方法
2.2.1 结合试验以确定靶点的相互作用
蛋白质组学技术,如亲和层析法和质谱法,已被用作识别越来越多药物的结合靶点的方法。在化学生物学验证靶点的时代,对药物的靶点和非靶点的分析以及药物的再利用已经成为自然的搭配。例如,细胞热稳定性试验(CETSA)技术已被引入,作为一种利用生物物理学方法在细胞中绘制靶点接触图的方法。利用生物物理学原理,预测具有适当细胞亲和力的类药物配体对目标蛋白的热稳定作用,来描绘细胞内的靶点结相互作用。
2.2.2 表型筛选
表型筛选可以确定在模型系统中显示出疾病相关效应的化合物,而无需事先了靶点。在药物再利用的背景下,如果所筛选的化合物是已获批准的或正在研究的药物,这可能表明可以随时寻求再利用的机会。通常情况下,体外表型筛选使用广泛的基于细胞的检测方法,采用96孔的格式。例如,Iljin及其同事在四个前列腺癌和两个非恶性前列腺上皮细胞系中,对4,910个类药物小分子化合物库进行了高通量细胞筛选。他们确定了双硫仑,是一种选择性的抗肿瘤剂。
药物再利用的挑战
正如前面所强调的,在药物再利用方面已经取得了显著的成功。已经在药物再利用方面取得了明显的成功。然而,再利用并不总是成功的;大多数是在III期试验阶段。与开发全新的药物一样,一些后期开发的失败显然是可以预期的,尽管这些失败应该不太可能是由于毒性造成的,因为候选药物的安全状况前面已经讲过了。然而,在再利用领域也有其他失败的原因,这与药物再利用的具体障碍有关,包括专利障碍、监管障碍和组织障碍。
3.1 专利障碍
为新的再利用适应症申请专利和实施专利权方面的困难是阻止药物再利用的关键障碍,因为它们对再利用产品的潜在利润有很大影响。只要新的医疗用途是新的和创造性的,就有可能在大多数主要医药市场上保护一个已知药物分子的新的再利用医疗用途。然而,许多潜在的再利用用途在科学文献或临床实践中已经是已知的。即使它们可能尚未通过临床试验被证明有效,但关于再利用用途的现有科学知识可能会限制获得专利保护的能力,除非专利权人能够以某种方式将其专利要求与公共领域中已经存在的信息相区别。为了获得新的再利用医疗用途的授权专利。
3.2 监管障碍
欧盟- 第2001/83/EC号指令(特别是第6、8(3)、10(3)和10(5)条)为再利用药物的药物申请提供了主要的法律依据。在欧洲,再利用药物的申请过程可以通过三种不同的途径进行:集中申请,分散申请或国家申请(相互承认)。- 申请应包含药物(理化、生物或微生物)试验、非临床(毒理学和药理学)试验和临床试验的信息。一些数据要求可以通过文献支持来满足数据要求。此外,对于参照参考药品数据的第10条(简略)申请,数据要求可以降低。- 安全性描述可由先前的临床经验(如试验数据或上市后数据)支持。- 所有申请都应附有风险管理计划。- 所有根据第8(3)条提出的申请都需要有儿科调查计划或豁免权,在申请前要与欧洲药品管理局(EMA)达成一致。- 可以使用变更申请为已批准的药物增加新的适应症。美国- 再利用药物的药品申请可以按照其中一种可能的监管途径提交,即第505(b)(1)条、第505(b)(2)条或第505(j)条。- 如果要对已经有批准的新药申请(NDA;或生物制品的生物制品许可申请(BLA))的产品进行小的改动(标签、新的剂量或强度等),公司必须提交补充NDA(sNDA;或生物制品的sBLA)。
3.3 生产中的组织障碍
制药公司正在意识到在其主要关注的疾病领域之外进行药物再利用的潜力,并与较小的生物技术公司和学术界展开合作。阿斯利康开放式创新平台(见相关链接)就是这样一个例子,它促进了外部合作,使药物再利用研究与通过转化、临床前实验和临床II期研究获得适合再利用的特征明确的化合物协同进行。然而,制药业的再利用可能会遇到一些组织上的障碍,特别是如果再利用的适应症不在组织的核心疾病领域内,或者该化合物在开发过程中已经停止,因此在研发部门内不再有一个 "活 "的项目来为新适应症提供专门支持。这意味着缺乏能够从事潜在药物再利用项目的人员,而且公司内部用于推进这一想法的资金和资源也有限。应对这些临床研究挑战的方法之一是通过合同生产组织、监管支持和药物警戒来利用外部资源进行药物供应,支持和药物警戒。
药物再利用的建议
考虑到上述药物再利用的机遇和挑战,我们最后提出了六项建议,以帮助实现药物再利用的全部潜力。
首先,需要有更好的数据分析综合平台。大数据的好处以及它如何帮助识别再利用的机会是显而易见的。然而,数据访问和整合仍然是一个瓶颈,特别是对于临床数据(包括病人病例记录中的临床医生笔记)。需要有先进的技术解决方案,以减少人工整理的需要,并帮助整合不同类型的全向性数据,从而使后续分析更加精细,并由更多的 "非专业人士 "以用户友好的格式进行分析。第二,需要改善对工业生产的临床前和临床化合物的获取途径。MRC和NIH-NCATS计划是正确研究的一步,但需要增加学术研究人员可以访问的化合物数量,理想情况是在大型图书馆中建立数据库。第三,有必要更多地获取II-IV期临床试验的数据。这可以让外部科学家在数据中挖掘新的发现,从而开启再利用的机会,特别是对已停止的项目。第四,应研究再利用药物的新的安全责任。持续需要确定与再利用药物相关的任何新的安全影响。这可能是由于药物与被重新利用的疾病之间新的相互作用、在新的人群中使用或给药时间的不同而产生的剂量安排的不同而产生的。(例如,慢性而非间歇性用药)。第五,需要为一般的药物再利用倡议提供更多的资助机会,包括资助适当的技术,支持化合物的使用和分享药物再利用库。还需要为特别是罕见疾病的药物再利用倡议提供创新的资金来源。最后,需要采取措施鼓励药物再利用,特别是解决上述的专利和监管障碍。这些措施可以包括为再利用的适应症提供更好的数据独占期,与非专利公司的特许权使用费安排或其他立法变化,以确保有足够的机会收回对药物再利用计划的投资。参考文献:
Pushpakom, S., Iorio, F., Eyers, P. et al. Drug repurposing: progress, challenges and recommendations. Nat Rev Drug Discov 18, 41–58 (2019). https://doi.org/10.1038/nrd.2018.168
版权信息
本文系AIDD Pro接受的外部投稿,文中所述观点仅代表作者本人观点,不代表AIDD Pro平台,如您发现发布内容有任何版权侵扰或者其他信息错误解读,请及时联系AIDD Pro (请添加微信号sixiali_fox59)进行删改处理。
原创内容未经授权,禁止转载至其他平台。有问题可发邮件至sixiali@stonewise.cn |
|