|
|
前言
药物在人体中起作用总结为两点:递送(delivery)和功能(function)。自科学家探究细胞基因治疗的深层机制,带来的革命性的强大疗效“function”面前,我们需要更加精准的“delivery”,将目标细胞或基因安全有效地递送到人体内,载体技术的突破能帮助研究人员和临床医生开发出强大的药物平台,并从根本上改变医学的面貌。细胞与基因治疗的核心就是载体,在近些年涌现出一波基于病毒载体的药物,相继获得监管部门的批准,从基于载体的癌症疗法到治疗具有改变生命结果的单基因疾病。在基于病毒载体的细胞与基因治疗领域,目前还面临着工艺开发质量控制的难度挑战。慢病毒载体(Lentivirus vector, LV)是目前分子及细胞生物实验中非常有效的工具,在基因转染方面有着许多独特的优势。我们将从慢病毒载体与其他病毒载体的比较、发展过程、临床进展以及慢病毒生产制备过程中的应用挑战展开研究论述。
<hr/>1. 病毒载体概述
1.1 载体是细胞与基因治疗的技术关键
细胞与基因治疗(CGT,Cell and Gene Therapy)是通过将特定的改变细胞功能的遗传物质引入患者体内来治疗包括遗传病和癌症最具前景的生命科学攻坚领域。可以分为细胞治疗技术和基因治疗技术。细胞治疗技术以体外治疗方式为主,包括提取患者的细胞或从同种异体来源中提取,通过携带治疗性转基因的载体进行基因修饰,在培养物中选择和扩增,以及输注将工程细胞重新引入患者体内。基因治疗技术则以体内细胞治疗方式为主,需要将携带治疗性转基因的载体直接施用到患者体内。有四种基本的基因治疗方法:
- 基因替代,递送功能基因以替代非工作基因;
- 基因沉默,使对细胞有毒的突变基因失活;
- 基因添加,“外来”或外源基因的过度表达以影响细胞功能;
- 基因编辑,对患者基因组中的基因进行永久性操作。
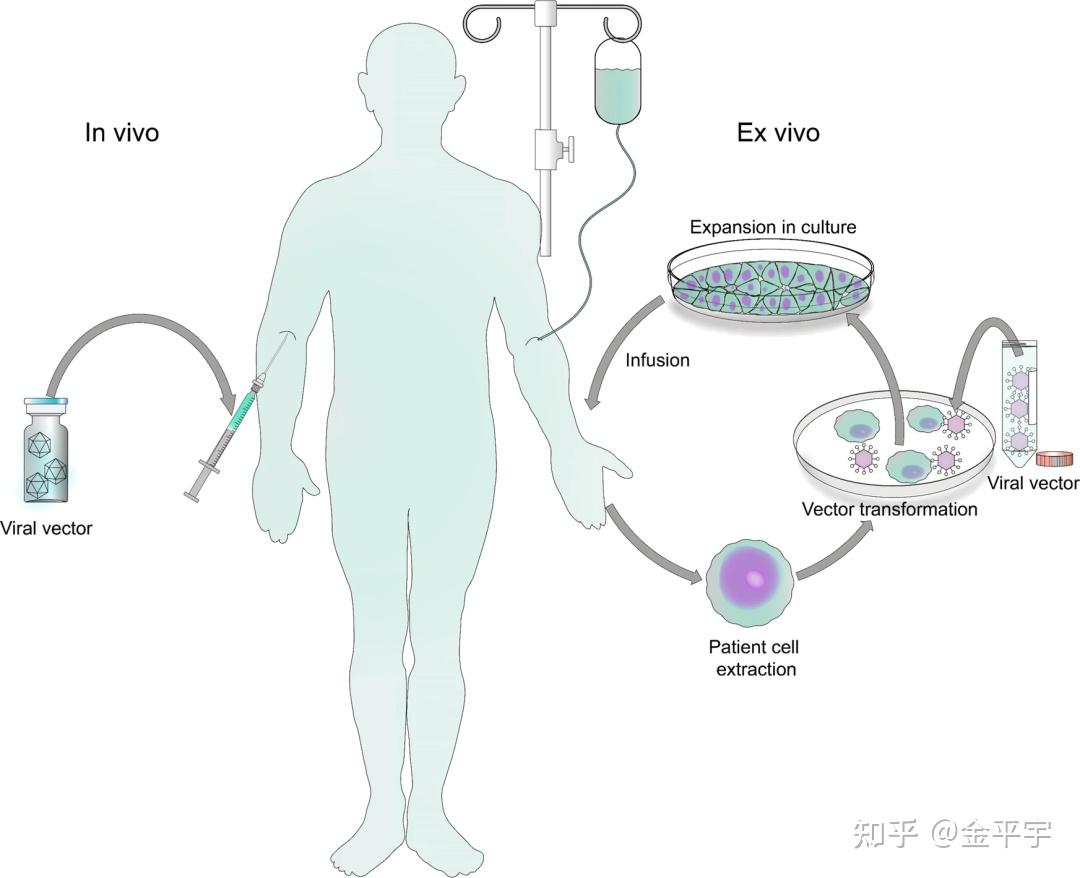
图:CGT治疗方法总结【来源:Signal transduction and targeted therapy 6.1 (2021)】
CGT的关键步骤是有效地将基因递送到目标组织或细胞中,这是由载体进行的。有两种类型的载体:病毒和非病毒。载体分为病毒和非病毒两大类,目前88%的在研基因治疗药物递送系统使用病毒载体。
病毒载体的特点是借助病毒远超于人类的进化史形成的高效穿透细胞膜的能力,具有高转导效率、靶向特定细胞、长期表达转基因,并具备被大规模生产的能力。
非病毒载体主要是出于对病毒安全性的担忧形成的替代方案,易于量产,细胞毒性、免疫原性和致突变性较低,但还存在递送效率低、转基因瞬时表达低,以及在颗粒均一性及稳定性的不足。未来一段时间主流的递送技术还是病毒载体。
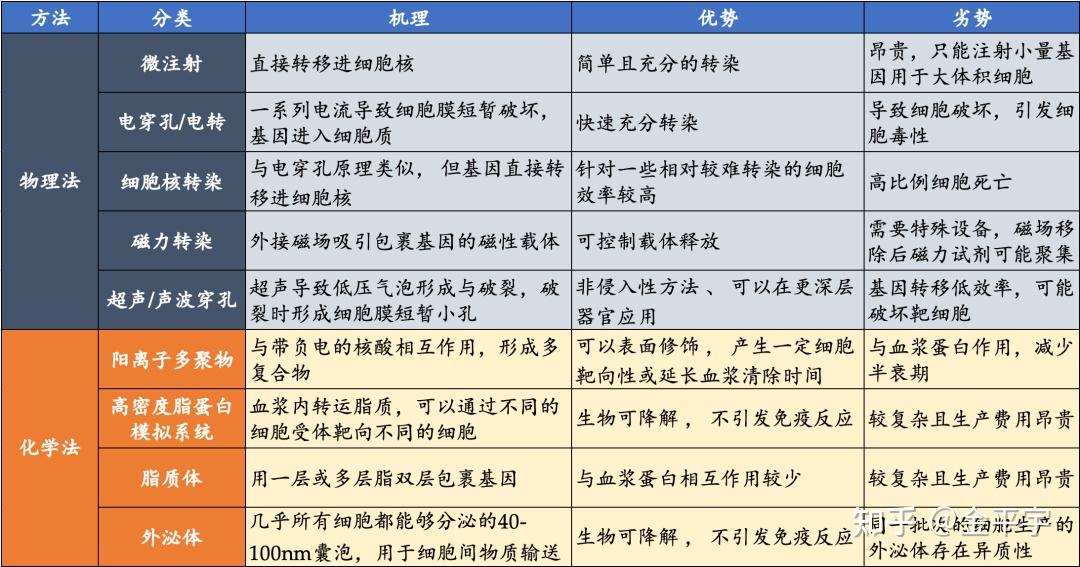
表:非病毒载体的分类特点及优劣势
1.2 病毒载体的分类特点
随着病毒生物学的发展,种类繁多的病毒载体已越来越成为向各种实验系统(如细胞系、原代细胞、组织脏器等)转运核酸的重要工具。除了在实验室的组织培养和动物模型生产中发挥重要作用,它们还被用于治疗遗传性疾病的临床试验中。
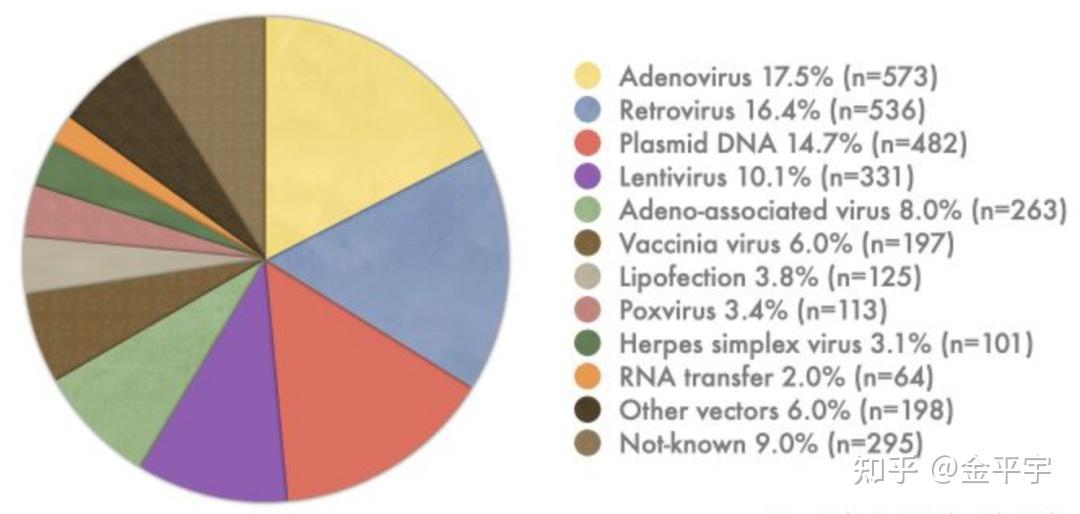
基因治疗临床试验中使用的载体个数及占比(截至2021年)【来源:The Journal of Gene Medicine Clinical Trial site】
目前主流的病毒载体系统主要包括慢病毒(LV)、腺相关病毒(AAV)、腺病毒(Ad)和γ-逆转录病毒(RV)。

表:四种主流病毒载体的分类特点
1.3 病毒载体的应用情况
慢病毒(Lentivirus, LV)
慢病毒因无严重的临床事故出现成为目前最安全的病毒载体选择之一。
慢病毒属于逆转录病毒科,但拥有比γ-逆转录病毒更为复杂的基因组,由于一般潜伏期较长,因此得名慢病毒。
大多数的逆转录病毒没有穿透核膜的能力,只能等待有丝分裂时进入核中。而慢病毒能够穿透核膜,感染的更广泛的细胞阶段,对分裂细胞和非分裂细胞都能实现高效的感染,因此在发展中慢病毒载体逐渐取代了原本的逆转录病毒载体体系。
慢病毒载体是多功能工具,具有能感染非分裂期细胞、容纳外源性目的基因片段大、稳定性强、免疫原性小等特点。这些病毒能够实现长期稳定的基因表达,并永久整合到宿主基因组中。
大量研究表明,相对其他病毒载体,慢病毒感染效率高,更容易感染一些较难感染的组织和细胞,其效率一般可以达到30%-95%以上。相比于腺病毒以及腺相关病毒,慢病毒容量更大,能携带更大、更复杂的基因组,并且具有整合转基因到宿主基因组的能力使产物稳定和长期的表达。慢病毒作为替代逆转率病毒的载体,保留了高表达效率和长表达时间的优点,还具备将其基因组整合到非分裂细胞中并进行转导,感染能力提升等优势,主要应用于体外基因治疗,占比已近7成,尤其是在CAR-T治疗领域,慢病毒的应用非常普及,远远多于其他载体。目前也有在体内基因治疗开展的临床的研究。对于以造血干细胞移植为唯一治疗手段的许多疾病,慢病毒基因疗法很有可能创造新的治疗前景。
Oxford BioMedica
慢病毒载体基因治疗的先驱,并且是诺华的CAR-T产品Kymriah生产慢病毒载体的唯一供应商。产品研发方面,凭借LentiVector®慢病毒载体递送技术,该公司与赛诺菲、GSK等一线药企建立了良好合作关系,具有庞大的资金来源,包括工艺开发和生物加工收入以及特许权使用费。此外,该公司针对眼科疾病、帕金森氏病在内的基因疗法的临床研究也在稳步推进中。
Bluebird Bio
蓝鸟是一家专注于使用慢病毒基因疗法以治疗严重遗传疾病的生物科技公司,有3个主要管线产品,分别为Beti-Cel(用于治疗β-地中海贫血)、Lovo-Cel(治疗镰状红细胞病)和Eli-Cel(治疗肾上腺脑白质营养不良)。今年8月份,美国FDA批准了蓝鸟公司的同类产品Zynteglo地贫基因治疗的药物上市,用于治疗输血依赖型非β0/β0型地贫患者,上市价格为280万美元,然而这个定价对于国内患者家庭而言几乎是不可逾越的屏障。
Orchard Therapeutics
旗下OTL-103是一种自体造血干细胞基因疗法,包括用编码Wiskott-Aldrich综合征(WAS)基因的慢病毒载体体外转染的CD34+细胞,旨在通过单次注射治疗Wiskott-Aldrich综合征。该疗法已获得FDA授予的孤儿药资格和罕见儿科疾病(RPD)资格。目前,评估疗效和安全性的3期临床试验正在进行中。
Mustang Bio
野马生物的慢病毒基因疗法MB-107和MB-207目前均处于1/2期临床试验阶段(NCT01512888;NCT01306019),用于治疗X连锁严重联合免疫缺陷症(XSCID),也被称为“泡泡男孩”病。这两个项目预计将在明年启动关键2期临床试验。
AVROBIO
致力于推进数项慢病毒基因疗法,针对包括法布里病、戈谢病、胱氨酸病和庞贝氏病在内的溶酶体贮积症。该公司设计了专有的第三代4质粒慢病毒载体系统,这是一种有效且经过验证的基因转移系统,可将基因稳定添加到患者自身的CD34 +细胞中。
Rocket Pharmaceuticals
致力于开发儿童罕见病基因疗法,近日在第28届欧洲基因与细胞治疗学会(ESGCT)年会上,报告了其慢病毒基因疗法RP-L201治疗I型白细胞粘附缺陷-I(LAD-I)的1/2期临床试验积极数据。
本导基因
2021年末,由中国人民解放军联勤保障部队第九二〇医院和上海本导基因技术有限公司合作开展的“慢病毒载体转导自体CD34+造血干细胞治疗输血依赖型β-地中海贫血的安全性和有效性研究”的临床实验已取得初步成效。这是国内首次报道基于慢病毒载体基因转导技术治疗β-地中海贫血的成功案例。
本导基因通过技术创新与工艺升级,不但在疗效上超越蓝鸟产品,成功治愈了两例双β0的地中海贫血患者,在成本上也得到了有效控制。目前本导基因正在积极推动地贫管线BD211的IND申报工作,加速推进药品的临床试验和上市速度,为广大患者提供一次治愈、价格合理的基因治疗产品。
腺病毒(Adenovirus, Ad)
腺病毒在上世纪末发生过一起严重的免疫反应致死,终结了第一波基因治疗热潮。
鸟氨酸氨甲酰基转移酶(OTC)缺乏症(OTCD)是一种罕见的X连锁遗传代谢病,是一种先天性尿素循环代谢障碍,当该酶系中一种酶丢失或者缺陷,氨就会积累在血液中,循环至大脑,引起高氨血症、脑病和呼吸性碱中毒,最终严重损伤大脑。每40000名出生婴儿中就有一名患有OTC的缺失。1999年,患有OTC缺乏症的18岁少年Jesse Gelsinger,在接受宾夕法尼亚大学人类基因治疗研究所所长Jim Wilson教授主导的腺病毒基因治疗临床实验后,发生严重免疫反应后死亡,成为第一个因基因治疗而死的人。
此后,美国FDA开始调查并严格审核基因治疗临床试验,当时基因治疗明星载体腺病毒也因此逐渐没落,基因治疗也因此沉寂了近20年时间。
在这之后腺病毒载体并没有因此完全退出历史舞台。相比于慢病毒,腺病毒搭载的基因导入后并不会整合到基因组上,因此不会有随机插入的风险。包装容量也是主流病毒载体中最大的,最高可以插入7.5kb的外源片段;并且腺病毒载体的感染效率非常高,感染后的表达速度也很快。这些特点促使用腺病毒开发疫苗,诱导强烈的免疫原性反应,可以在注射后的短期内大量表达抗原蛋白,并在一段时间后随着细胞的分裂和复制被代谢掉。腺病毒疫苗相对研发生产过程简单,在新冠疫情中,康希诺生物、阿斯利康和强生都选择了腺病毒载体技术路线的新冠疫苗。但是在实际使用中,腺病毒还是出现了安全性问题。强生和阿斯利康的疫苗都屡有安全性问题爆出。康希诺生物的疫苗是三款产品中安全性表现最好的一款,基本没有严重的安全问题发生,但是接种后的不良反应发生率也显著高于广泛使用的灭活疫苗。
此外,腺病毒载体还有在溶瘤病毒上的改造用于癌症治疗。未来还需要继续优化载体的安全性。
腺相关病毒(Adeno-associated virus, AAV)
Jesse Gelsinger因腺病毒基因治疗死亡的悲剧发生后,Jim Wilson缩小了实验室的规模,将精力放在了寻找更加安全的病毒载体上,最终在2016年2月,他们发现并推广使用了腺相关病毒AAV。James Wilson团队用AAV8血清型载体将作为剪切工具的核酸酶Cas9特异性导入肝细胞中。另一个载体将gRNA带到特异性DNA靶位点,从而达到定点突变。
AAV具有安全性好、宿主细胞范围广和在体内表达时间长等特点,是基因治疗非常重要的载体之一,是目前唯一一个NIH评级为RG1的病毒载体,迄今从未发现野生型AAV致病;重组AAV去除了野生型AAV基因组的96%,进一步保证了安全性;由于AAV不插入基因组,因而没有致癌性;其本身的免疫原性又基本不会引起免疫排斥,相对其他病毒优势非常明显。
但同时AAV载体的弊端也比较明显,由于AAV的包装容量过小,对基因大小限制较多,其应用场景有限。再者感染到表达的时间比较长,而且使用AAV作为载体的基因治疗需要消耗大量的病毒,并可能需要多次注射,如何降低生产成本也成为目前各方关注的焦点。
逆转录病毒(Retrovirus, RV)
γ逆转录病毒,通常称为逆转录病毒(RV),是单链RNA病毒,在宿主细胞内直接被当做mRNA合成早期蛋白,同时依赖RNA聚合酶合成双链,再转录成后来的致病mRNA。由于逆转录病毒能够随机插入宿主细胞基因组并稳定整合,它被广泛用于基因治疗中,并取得很大的成功。
但其缺点也很明显。由于其倾向于插入基因第一个内含子和转录起始位点,它相对慢病毒更容易引起插入性随机突变。在1997年,伦敦医生尝试用逆转录病毒,莫罗尼小鼠白血病病毒,治疗X染色体上的IL2RG基因突变缺陷导致的X连锁重症联合免疫缺陷症(SCID-X1),然而,由于其插入和破坏的基因变成了人类基因LMO2(LIM domain only 2)导致基因的异常激活,从而引发数例白血病。这次的事件也与1999年腺病毒治疗Jesse Gelsinger导致死亡的事件一齐成为基因治疗历史上的两大事故。这两起悲剧无时无刻不提示人们对于病毒载体安全性的思考和关注。
<hr/>2. 慢病毒载体发展过程
CGT核心载体:慢病毒载体系列研究(2)慢病毒载体发展过程 - 知乎 ( @金平宇 )
<hr/>Reference:
- Perry, Christopher, and Andrea CME Rayat. &#34;Lentiviral vector bioprocessing.&#34; Viruses 13.2 (2021): 268.
- Bulcha, Jote T., et al. &#34;Viral vector platforms within the gene therapy landscape.&#34; Signal transduction and targeted therapy 6.1 (2021): 1-24.
- Anguela, Xavier M., and Katherine A. High. &#34;Entering the modern era of gene therapy.&#34; Annu Rev Med 70.1 (2019): 273-288.
- Magrin, Elisa, Annarita Miccio, and Marina Cavazzana. &#34;Lentiviral and genome-editing strategies for the treatment of β-hemoglobinopathies.&#34; Blood, The Journal of the American Society of Hematology 134.15 (2019): 1203-1213.
- Ramezani, Ali, and Robert G. Hawley. &#34;Overview of the HIV‐1 lentiviral vector system.&#34; Current Protocols in Molecular Biology 60.1 (2002): 16-21.
- Johnson, Nathan M., et al. &#34;HIV-based lentiviral vectors: origin and sequence differences.&#34; Molecular Therapy-Methods & Clinical Development 21 (2021): 451-465.
|
|